Starten met Ofev
Starten met Ofev
Start de behandeling met Ofev direct na IPF diagnose1
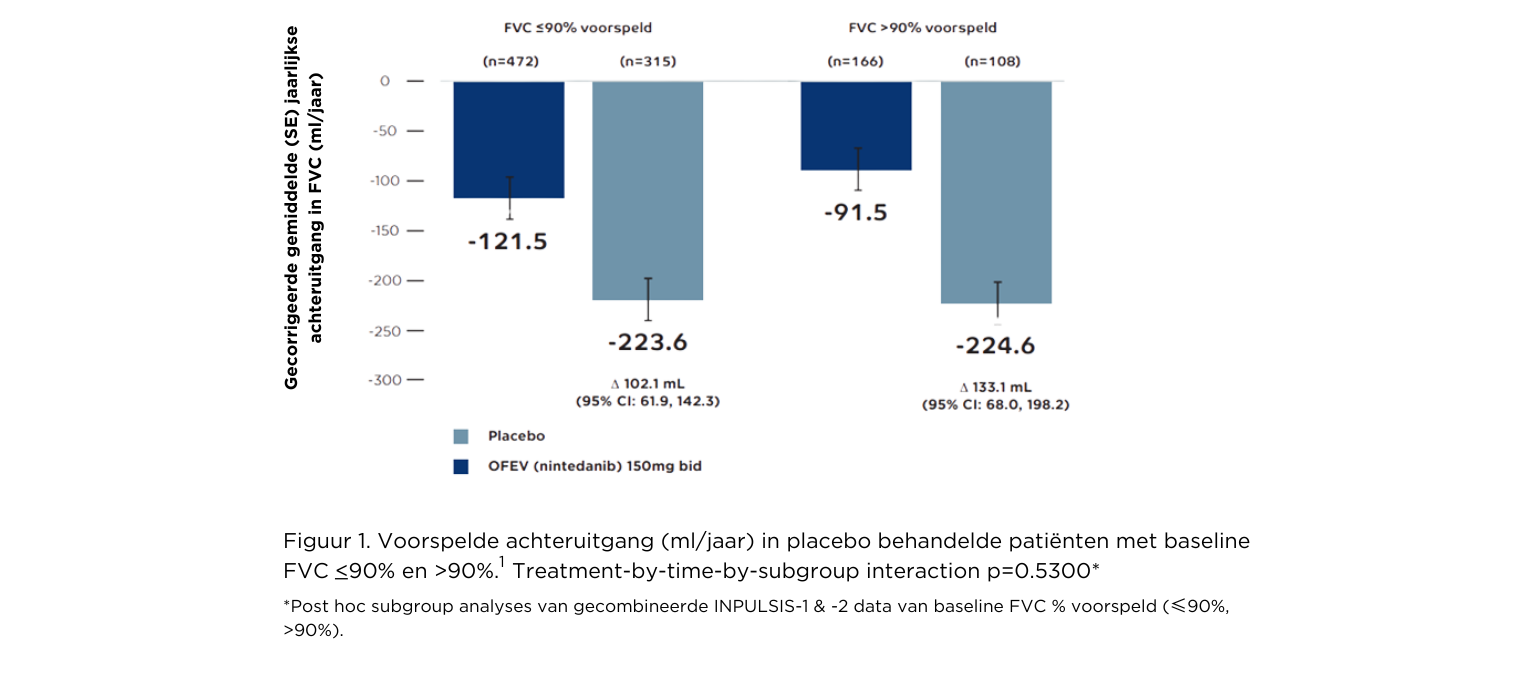
Het is van belang om de behandeling met Ofev direct te starten bij de diagnose IPF, ongeacht de baseline FVC-waarde.1 Figuur 1 laat een vergelijkbaar effect van Ofev 150mg tweemaal daags zien bij een behouden longfunctie (FVC ≤90% van voorspeld) of een verminderde longfunctie (FVC>90% van voorspeld).1 Ook bij een diffusiecapaciteit voor koolmonoxide (DLCO) ≤40% van voorspeld of een DLCO >40% van voorspeld is een vergelijkbaar effect op de longfunctie te zien bij het gebruik van Ofev 150mg tweemaal daags. 2 De achteruitgang van de longfunctie is duidelijk te zien bij de placebogroep.
Ook kwetsbare patiënten hebben baat bij een behandeling voor ILD3
De helft van de ILD-patiënten wordt beschouwd als kwetsbaar en heeft een 1,5 keer hoger risico op vroegtijdig overlijden.3,4 Kwetsbaarheid kan ook gerelateerd zijn aan verminderde longfunctie (lagere FVC en DLCO).3,5 Ook deze kwetsbare patiënten kunnen baat hebben bij een behandeling om ILD-progressie te vertragen.3
Ofev vermindert consistent de afname van longfunctie bij IPF, ongeacht de hoeveelheid comorbiditeiten en leeftijd.6 Ook bij PPF- patiënten is Ofev effectief, ongeacht BMI.7 Het is wel belangrijk het gewicht van uw patiënt in de gaten te houden vanwege het risico op gewichtsverlies.8
Bij patiënten met aan bindweefselziekte gerelateerde ILD (CTD-ILD) dragen immunosuppressiva mogelijk bij aan hun kwetsbaarheid.3 Immunosuppressiva hebben geen invloed op de effectiviteit en verdraagbaarheid van Ofev.9,10 Het is aangetoond dat Ofev de FVC-afname vertraagt en een consistent verdraagbaarheidsprofiel heeft, ongeacht of patiënten anti-reumatische geneesmiddelen (DMARD’s)of glucocorticoïden innemen.9,10
REFERENCES:
-
Kolb M, Richeldi L, Behr J, et al. Nintedanib in patients with idiopathic pulmonary fibrosis and preserved lung volume. Thorax. 2017;72(4):340-346. doi:10.1136/thoraxjnl-2016-208710
-
Brown KK, Flaherty KR, Cottin V, et al. Lung function outcomes in the INPULSIS(®) trials of nintedanib in idiopathic pulmonary fibrosis. Respir Med. 2019;146:42-48. doi:10.1016/j.rmed.2018.11.012
-
Guler SA, Ryerson CJ. Frailty in patients with interstitial lung disease. Curr Opin Pulm Med. 2020;26(5):449-456. doi:10.1097/MCP.0000000000000692
-
Farooqi MAM, O’Hoski S, Goodwin S, et al. Prevalence and prognostic impact of physical frailty in interstitial lung disease: A prospective cohort study. Respirology. 2021;26(7):683-689. doi:10.1111/RESP.14066
-
Sheth JS, Xia M, Murray S, et al. Frailty and geriatric conditions in older patients with idiopathic pulmonary fibrosis. Respir Med. 2019;148:6-12. doi:10.1016/j.rmed.2019.01.008
-
Glaspole I, Bonella F, Bargagli E, et al. Efficacy and safety of nintedanib in patients with idiopathic pulmonary fibrosis who are elderly or have comorbidities. Respir Res. 2021;22(1):1-10. doi:10.1186/s12931-021-01695-y
-
Jouneau S, Crestani B, Thibault R, et al. Analysis of body mass index, weight loss and progression of idiopathic pulmonary fibrosis. Respir Res. 2020;21(1):1-11. doi:10.1186/s12931-020-01528-4
-
Kreuter M, Bendstrup E, Jouneau S, et al. Weight loss and outcomes in subjects with progressive pulmonary fibrosis: data from the INBUILD trial. Respir Res. 2023;24(1):1-9. doi:10.1186/s12931-023-02371-z
-
Cottin V, Richeldi L, Rosas I, et al. Nintedanib and immunomodulatory therapies in progressive fibrosing interstitial lung diseases. Respir Res. 2021;22(1):1-9. doi:10.1186/s12931-021-01668-1
-
Matteson EL, Kelly C, Distler JHW, et al. Nintedanib in Patients With Autoimmune Disease–Related Progressive Fibrosing Interstitial Lung Diseases: Subgroup Analysis of the INBUILD Trial. Arthritis Rheumatol (Hoboken, N.j). 2022;74(6):1039. doi:10.1002/ART.42075
PC-NL-106386
